匯總:聚合物鋰電池補鋰幾種方法
在聚合物鋰電池的首次充電過程中,有機電解液會在石墨等負極表面還原分解,形成固體電解質相界面(SEI)膜,永久地消耗大量來自正極的鋰,造成首次循環的庫侖效率(ICE)偏低,降低了聚合物鋰電池的容量和能量密度。

現有的石墨材料有5%~10%的首次不可逆鋰損耗,而對于高容量負極材料,首次鋰損耗甚至更高(硅的不可逆容量損失達15%~35%)。為了解決這個問題,人們研究了預鋰化技術。通過預鋰化對電極材料進行補鋰,抵消形成SEI膜造成的不可逆鋰損耗,以提高聚合物鋰電池的總容量和能量密度。
本文通過從從負極補鋰和正極補鋰兩個方向,綜述近年來預鋰化技術的研究進展。
一、負極補鋰技術
常見的預鋰化方式是負極補鋰,如鋰箔補鋰、鋰粉補鋰等,都是目前重點發展的預鋰化工藝。此外,還有利用硅化鋰粉和電解鋰鹽水溶液來進行預鋰化的技術。
1.鋰箔補鋰
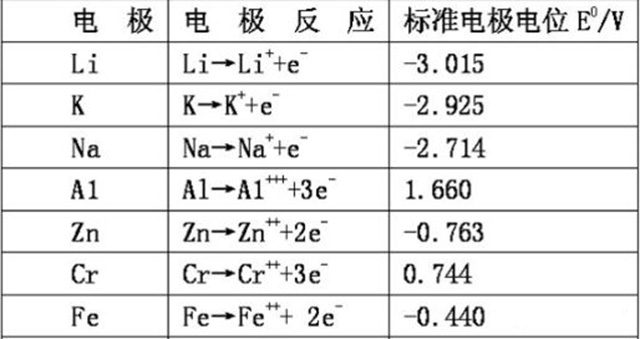
鋰箔補鋰是利用聚合物鋰電池自放電機理進行補鋰的技術。金屬鋰的電位為-3.05V(vs.SHE,標準氫電極),在所有電極材料中最低。由于電勢差的存在,當負極材料與金屬鋰箔接觸時,電子自發地向負極移動,伴隨著Li+在負極的嵌入。
在生長于不銹鋼基底的硅納米線(SiNWs) 負極上滴加電解液,再與鋰金屬箔直接接觸,進行補鋰。對補鋰后的負極進行半電池測試,發現: 未補鋰的SiNWs開路電壓(OCV) 為1.55V,在0.01~1.00 V 首次0.1 C 放電的嵌鋰比容量為 3800 mAh /g;補鋰后的SiNWs OCV為 0.25 V,首次嵌鋰比容量為1600mAh /g。OCV 和嵌鋰比容量的變化說明: 補鋰后,Si 已經部分與 Li 發生了反應。
將錫碳(Sn-C) 負極與被電解液浸潤的鋰箔直接接觸180min,進行補鋰。用半電池以 80 mA/g 在0. 01 ~ 2. 00V 內測試,補鋰后 Sn-C 的不可逆比容量由 680mAh /g( 63% ) 減少到 65 mAh /g( 14% ) 。將該負極與 LiNi0. 45Co0. 1Mn1. 45O4 構成全電池,1. 0 C 倍率在 3. 1 ~ 4. 8 V 下測試的 ICE 接近100% ,且循環穩定,倍率性能較好; 5. 0 C 放電的比容量達到 110 mAh /g,較0. 2 C 的放電容量僅下降了 14% 。
盡管與鋰箔直接接觸,可以實現負極預鋰化,但預鋰化的程度不易精確控制。不充分的鋰化,不能充分提高 ICE;而補鋰過度,可能會在負極表面形成金屬鋰鍍層。
利用外部短路,通過鋰箔對氧化硅負極( c-SiOx ) 補鋰。對比實驗表明: 外短路電路中的電阻為 100 Ω、短路時間 30min 時,可實現 ICE 的最大化。對補鋰前后的 c-SiOx 進行半電池測試,以 0.07 C 在 0.01 ~ 1.50 V 的前 5 次循環,補鋰前電極的庫侖效率依次為 73.6% 、94.7% 、96.6% 、97.5% 和98. 0%; 補鋰后電極的庫侖效率依次為 94.9% 、95.7% 、97.2% 、97.9% 和 98.3% 。將 c-SiOx 與 LiNi0. 8 Co0. 15 Al0. 05 O2構成全電池,用 10 mA/g 的電流在 2. 5 ~ 4. 2 V 測試,補鋰后電池的放電比容量由補鋰前的 106.33 mAh /g 上升到 165.09mAh /g,ICE 從 58.85% 提高到 85.34% 。
對鋰箔補鋰的安全性進行了改善,設計的活性材料/聚合物/鋰金屬三層結構負極可在環境空氣( 相對濕度為 10%~30% ) 中穩定 30~60 min,足夠負極進行加工。三層結構分別為: 在銅箔上通過電化學沉積的金屬鋰層,對鋰層進行包覆聚甲基丙烯酸甲酯( PMMA) 保護層以及活性材料層。改變鋰層的厚度,可以控制補鋰程度。向電池中注入電解液溶解 PMMA 后,鋰層和活性物質直接接觸,即可完成預鋰化。用 0. 1C 在 0. 01 ~ 1. 00 V 測試,利用該三層結構補鋰后的石墨,ICE 從 92.0% 上升到 99.7%; 純硅負極補鋰后,首次充放電幾乎沒有容量損失。盡管利用鋰箔進行補鋰有較好的效果,但補鋰過程需要在臨時的電池或電化學裝置中完成,難以擴大規模。
2.穩定化鋰金屬粉末( SLMP)
鋰粉補鋰是富美實公司提出的,開發的 SLMP 比容量高達 3600 mAh /g,表面包覆了 2% ~ 5% 的碳酸鋰( Li2CO3 ) 薄層,可在干燥環境中使用。將 SLMP 應用于負極預鋰化,主要有兩種途徑: 在合漿過程中添加,或直接添加到負極片表面。
常規的聚合物鋰電池負極合漿,使用聚偏氟乙烯( PVDF) /甲基吡咯烷酮( NMP) 或丁苯橡膠( SBR) + 羧甲基纖維素( CMC) /去離子水體系,但 SLMP 與極性溶劑不兼容,只能分散于己烷、甲苯等非極性溶劑中,因此不能在常規的合漿過程中直接加入。L. Wang 等采用 SBR-PVDF/甲苯體系,可將 SLMP 直接混合在石墨電極漿料中。首先將石墨、PVDF 在 NMP 溶劑中混合,烘干后形成 PVDF 包覆的石墨; 再將 SLMP、PVDF 包覆的石墨、導電炭黑在甲苯中混合; 最后加入 SBR。經過 SLMP 對負極的預鋰化,在 0.01 ~ 1.00 V、0.05 C 的條件下,電池的ICE 從 90.6% 提高到 96.2% 。
與在合漿過程中加入相比,SLMP直接加載到干燥的負極表面更簡單易行。使用 SLMP 對硅( Si) -碳納 米 管 ( CNT) 負極進行預鋰化,將質量分數為 3% 的SLMP/甲苯溶液滴在 Si-CNT 負極表面,待甲苯溶劑揮發后,進行壓片、激活。預鋰化后,負極的首次不可逆容量減少了20% ~ 40% 。
將 SLMP 分散于含有 1% SBR/聚苯乙烯的二甲苯溶液中,形成穩定的 SLMP 漿料。將 SLMP 漿料涂覆在干燥的負極表面,來實現對石墨、SiO 等負極的預鋰化。經過預鋰化,石墨|鎳鈷錳三元材料( NCM) 全電池以 0.1 C 在 3.0~ 4.2 V 測試,ICE 由 82.35% 提高到 87.80% ; SiO | NCM 全電池的 ICE 從未鋰化的 56.78% 提高到預鋰化后的 88.12% 。
3.硅化鋰粉
與微米尺寸的 SLMP 比,納米硅化鋰粉( LixSi) 的尺寸( 100 ~ 200 nm) 更小,更有利于在負極中的分散。此外 LixSi已處于膨脹狀態,循環過程中的體積變化不會對整個電極的結構造成影響。目前,對 LixSi 補鋰添加劑的研究較少,對 LixSi 的補鋰性能和穩定性改善進行了研究。在氬氣氣氛下,利用硅與金屬鋰在 200 ℃ 下的合金化反應,合成表面包覆 Li2O 的 LixSi 材料。半電池體系以 0.05 C 在 0.01 ~1.00 V 充放電,添加 15% LixSi 后,硅負極的 ICE 從 76% 提高到 94% ; 添加 9% LixSi 的中間相炭微球( MCMB) 的 ICE從 75% 提高到 99% ; 添加 7% LixSi 的石墨負極的 ICE 從87% 提高到 99% 。在全電池體系下,添加 7% LixSi 的石墨 |LiFePO4 電池的 ICE 從 77.6% 上升到 90.8% ,并在隨后的循環測試中具有更高的容量。
合成的 LixSi 補鋰性能較好,但僅能在干燥空氣中保持相對穩定性,在露點-50 ℃ 的干燥空氣中暴露 5 d 后,容量衰減 30% ,在空氣環境中完全失活。為了提高 LixSi 的穩定性,可采用 1-氟癸烷在顆粒表面還原,形成致密的包覆層。包覆后的 LixSi 在干燥空氣中放置 5 d 后,幾乎無衰減,在相對濕度 10% 的空氣中放置 6 h 后,在 0.01 ~ 1.00 V、0.02 C 的條件下,比容量依然高達 1604 mAh /g,容量保持率達到 77% 。在石墨負極中添加 5% 進行補鋰,在 0.005 ~1.500 V、0.05 C 的條件下,ICE 從 87.0% 增加到 96.7% 。為了進一步提高 LixSi 的穩定性,可使用 SiO、SiO2 取代 Si 作為原料,合成 LixSi-Li2O 復合材料。該復合材料在相對濕度40% 的空氣中放置 6 h 后,在 0.01 ~ 1.00 V、0.02 C 的條件下,比容量高達 1240 mAh /g。兩種原料合成的 LixSi-Li2O 復合材料,均表現出優異的補鋰性能。
4.電解鋰鹽水溶液進行補鋰
無論是使用鋰箔、SLMP還是硅化鋰粉來補鋰,都要涉及金屬鋰的使用。金屬鋰價格高、活性大,操作困難,儲存與運輸需要高額的費用用于保護。如果補鋰過程不涉及金屬鋰,可以節約成本,提高安全性能。通過在電解池中電解 Li2SO4 水溶液來對硅進行補鋰,犧牲電極為浸入Li2SO4中的銅線,補鋰反應如式(1)所示:

以 1 A/g 的電流電解 4.2 h,補鋰后的 MnOx | Si 全電池在 0.5 ~ 3.8 V 下測試,0.5 C、1.0 C、2.0 C、4.0 C 和8.0 C 比容量分別為 160 mAh /g、136 mAh /g、122 mAh /g、108 mAh /g和 92 mAh /g。
二、正極補鋰技術
與高難度、高投入的負極補鋰相比,正極補鋰簡便得多。典型的正極補鋰是在正極合漿過程中添加少量高容量材料,在充電過程中,Li+ 從高容量材料中脫出,補充首次充放電的不可逆容量損失。目前,作為正極補鋰添加劑的材料主要有: 富鋰化合物、基于轉化反應的納米復合材料和二元鋰化合物等。
1.富鋰化合物
使用富鋰材料 Li1 + x Ni0. 5 Mn1. 5O4 來補償 Si-C| LiNi0. 5Mn1. 5O4 全電池的不可逆容量損失。使用混合正極的電池以 0.33 C 在 3.00 ~ 4.78 V 循環 100 次的容量保持率為 75% ,而使用純 LiNi0.5 Mn1. 5 O4 正極的電池僅為51% 。此外,使用混合正極的 Si-C | LiNi0.5 Mn1.5O4 電池的能量密度,比石墨| LiNi0.5Mn1.5O4 電池增加了 25% 。
Li2NiO2 也可作為正極補鋰添加劑使用,但在空氣中的穩定性較差。使用異丙醇鋁對 Li2NiO2 進行改性,合成了在空氣中穩定的氧化鋁包覆的 Li2NiO2 材料,補鋰效果優異。未添加的 LiCoO2 | 石墨全電池,在 2.75 ~ 4.20V、0.2 C 條件下的 ICE 為 92% ,添加了 4% Li2NiO2 的電池,容量幾乎沒有損失,且倍率性能不受添加劑的影響。
在 LiCoO2 正極中添加 Li5FeO4 ( LFO) ,補償硬碳負極在首次充電過程中的容量損失。半電池測試顯示:添加 7% LFO 的 LiCoO2 正極 0.1 C 首次充放電( 2.75 ~ 4.30V) 比 容 量 分 別 為 233 mAh /g、160 mAh /g,不可逆容量占31% ,足以補償硬碳 22% 的首次不可逆容量損失。全電池測試( 2.75 ~ 4.30 V、0.05 C) 結果表明: 添加 7% LFO 的 LiCoO2 |硬碳全電池的可逆容量增加了 14% ,能量密度提高了10% ,循環性能也得到改善,全電池循環 50 次后的比容量保持率從不到 90% 提高到高于 95% 。添加 LFO 的 LiCoO2 正極,合漿、涂覆等過程需要在惰性氣氛中進行,LFO 在空氣環境中的穩定性有待提高。
2.基于轉化反應的納米復合材料
盡管富鋰化合物作為補鋰添加劑取得了一定的效果,但首次的補鋰效果仍受限于較低的比容量。基于轉化反應的納米復合材料,由于存在較大的充/放電電壓滯后,在電池首次充電過程中可貢獻出大量的鋰,而嵌鋰反應在放電過程中卻不能發生。
研究 M/氧化鋰( Li2O) 、M/氟化鋰( LiF) 、M/硫化鋰( Li2 S) ( M = Co、Ni 和 Fe) 作為正極補鋰添加劑的性能。M/Li2O 通過在氬氣氣氛下混合MxOy 和熔融鋰合成。合成的納米 Co /納米 Li2O( N-Co /N-Li2O) 復合材料以 50 mA/g 在 4.1 ~ 2.5 V 循環,首次充電的比容量達 619 mAh /g,放電比容量僅為 10 mAh /g;N-Co /NLi2O 在環境空氣中暴露 8 h 后,脫鋰比容量僅比初始值小了51 mAh /g,放置 2 d 后,脫鋰比容量仍有 418 mAh /g,表明 NCo /N-Li2O 具有良好的環境穩定性,可與商業化電池的生產過程兼容。與 N-Co /N-Li2O 類似,N-Ni /N-Li2O、N-Fe /N-Li2O也有較高的充電比容量( 分別為 506 mAh /g 和 631 mAh /g)和很低的放電比容量( 分別為 11 mAh /g 和 19 mAh /g) ,補鋰性能優異。
LiF的鋰含量高、穩定性好,是一種潛在的正極補鋰材料。利用轉化反應構造的M/LiF納米材料,可以克服 LiF 電導率和離子導率低、電化學分解電位高、分解產物有害等問題,使 LiF 成為一種優良的正極補鋰添加劑。LiF/Co 在4.2 ~ 2.5 V 的脫鋰比容量高達 520 mAh /g,嵌鋰比容量僅有4 mAh /g,表明 LiF/Co 的補鋰能力達到 516 mAh /g。LiF/Fe在 4.3 ~ 2.5 V 的脫鋰比容量為 532 mAh /g,嵌鋰比容量為 26mAh /g,表 明 LiF/Fe 的補鋰能力達到 506 mAh /g。添 加4.8% LiF/Co 的 LiFePO4 | Li 半電池,以 0.1 C 在 2.5 ~ 4.2 V首次充電的比容量達到 197 mAh /g,比未添加 LiF/Co 電池的164 mAh /g 增加了 20.1% ,放電比容量相近,循環穩定性不受添加劑的影響。
Li2S的理論容量達到1166 mAh /g,但作為補鋰添加劑使用,仍有很多問題需要解決,如與電解液的兼容性、絕緣、環境穩定性差等。研究發現,將金屬引入 Li2 S,構成 L2 S /M復合 材 料,可解決這些問題。CoS2 與 金 屬 Li 合 成 的Li2 S /Co,補鋰容量達到 670 mAh /g。添加 4.8% Li2 S /Co 的LFP 電極,在 2.5 ~ 4.2 V 下,用 0.1 C 首次充電的比容量為204 mAh /g,比沒有添加的電極高了 42 mAh /g。FeS2 與金屬Li 合成的 Li2 S /Fe,補鋰容量達到 480 mAh /g。盡管補鋰容量低于 Li2 S /Co,但原材料 FeS2 的資源豐富且價格低廉,因此Li2 S /Fe 的商業化應用前景更好。盡管較富鋰化物有更高的補鋰容量,但基于轉化反應的納米復合材料在首次補鋰后,會殘余沒有活性的金屬氧化物、氟化物和硫化物等,降低電池的能量密度。
3.二元鋰化合物
與富鋰氧化物( 約 300 mAh /g) 、轉化反應復合材料( 500~ 700 mAh /g) 相比,二元鋰化合物的理論比容量要高得多。Li2O2、Li2O 和 Li3N 的理論比容量分別達到 1168 mAh /g、1797 mAh /g 和 2309 mAh /g,只需要少量的添加,就可實現類似的補鋰效果。理論上,這些材料在補鋰后的殘余物是O2、N2 等,可在電池形成 SEI 膜過程中排出的氣體。
將商業化的 Li3N 研磨成粒徑為 1 ~ 5 μm的粉體,用作補鋰添加劑。半電池體系下,添加了 1% 和 2%Li3N 的 LiCoO2 電極,以 0.1 C 在 3.0 ~ 4.2 V 的首次充電比容量分別為 167.6 mAh /g 和 178.4 mAh /g,較純 LiCoO2 上升了 18.0 mAh /g、28.7 mAh /g。LiCoO2 | SiOx /C@ Si 全電池在添加 2% Li3N 后的,以 0.5 C 在 1.75 ~ 4.15 V 下的放電容量較未加入添加劑的全電池上升了 11% 。為了解決混合電極導電性的問題,將 Li3N 沉積在 LiCoO2 電極的表面,可減小對電極導電率的影響。正極表面沉積 5% 添加劑的全電池,放電比容量為 126.3 mAh /g,較未加添加劑的電池提高了 14.6mAh /g,而倍率性能與循環性能相似。此外,將 Li3N 負載在干燥的電極表面,可避免 Li3N 與合漿溶劑(如甲基吡咯烷酮)不兼容的問題。
將商業化 Li2O2 與 LiNi0. 33 Co0. 33 Mn0. 33 O2(NCM) 混合使用,補償石墨負極首次充電過程中的鋰損失。混合電極中的 NCM 起到了活性材料和催化劑的雙重作用。為了高效地催化分解 Li2O2,在正極中加入 1% NCM-6 h( 球磨 6 h 得到的 NCM) 。石墨 | NCM/NCM-6 h /2% Li2O2全電池在 2.75 ~ 4.60 V 充放電,0.1 C 首次可逆比容量為 207.1mAh /g,較石墨 | NCM 全電池提高了 7.8% ; 0.3 C 可逆比容量為 165.4 mAh /g,較石墨 | NCM 全電池提高了 20.5% 。測試顯示,Li2O2 分解釋放的氧氣會消耗全電池中有限的 Li+ ,導致添加 Li2O2 的全電池存在明顯的容量衰減,但在排出氣體后,容量即可得到恢復。電池在實際生產過程中的首次充電是在開放體系中進行的,密封前會排出形成 SEI 膜和一些副反應產生的氣體,因此可減小 O2 釋放造成的影響。
研究微米尺寸的 Li2O 作為正極補鋰添加劑的效果,添加 20% Li2O 的 SiO-SnCoC| Li1.2Ni0. 15Mn0.55Co0.1O2 全電池,以 10 mA/g 在 2.0 ~ 4.5 V 循環的首次放電比容量由 176 mAh /g 上升到 254 mAh /g。實驗結果表明: 富鋰材料 Li1.2Ni0.15Mn0.55Co0.1O2 充當了活性材料和催化劑的雙重角色。
三、結論
對比兩種聚合物鋰電池補鋰方法,負極補鋰路線補鋰試劑的( 鋰箔、鋰粉和硅化鋰粉) 容量高,但操作復雜、對環境要求高;通過在正極中添加補鋰添加劑的正極補鋰路線勝在安全穩定性高,與現有電池生產工藝兼容性好。
本文鏈接:http://www.qhgfjy.com.cn{dede:field.arcurl/}
諾信新聞,諾信公司新聞,鋰電池行業新聞,展會新聞
下一篇:低溫環境下鋰離子動力電池性能分析









