鋰電池廠家分析:鋰電池電極配方如何確定
鋰離子電池的正、負極極片設計參數主要包括活性物質負載、孔隙率、厚度以及活性物質、粘合劑和導電添加劑之間的比例。在電極配方方面已經報道了很多,比如石墨-LFP體系,就有40多種配方,活性材料的比例從60%到95%,粘合劑的比例從2%到25%,導電添加劑的比例從3%到30%,這些配方范圍特別大。而在鋰電池廠家,電極配方也是非常機密的,無論技術交流還是具體合作,各單位也極少涉及到具體的材料體系和配方。
那么,電極配方到底有什么理論指導嗎?各廠家又是怎么確定具體配方的?我所經歷的情況,基本都是通過大量實驗,優化總結的電極配方。今天分享一點具體內容,拋磚引玉,歡迎大家討論。
鋰離子電池極片可看成一種復合材料,主要由以下幾部分組成:(1)活性物質顆粒,嵌入或脫出鋰離子,正極顆粒提供鋰源,負極顆粒接受鋰離子;(2)導電劑和黏結劑相互混合的組成相(碳膠相),粘結劑連結活物質顆粒,涂層與集流體,導電劑導通電子;(3)孔隙,填滿電解液,這是極片中鋰離子傳輸的通道。
電極中活性物質、導電劑和粘結劑之間的比例以及它們的分布狀態會影響電子、離子的傳輸,電極界面的電化學反應等,從而影響電池性能。
理想的電解微觀結構如圖1所示:導電劑和粘結劑充分分散,均勻分布活性物質顆粒表面,導電劑相互連通形成電子傳輸網絡,粘結劑分布均勻,確保顆粒涂層的結合強度和機械穩定性高,活性物質顆粒保持原始形貌并分散均勻,整齊排列,形成從電極表面到集流體的垂直孔道,確保電解液充分浸潤,實現鋰離子的快速傳導。
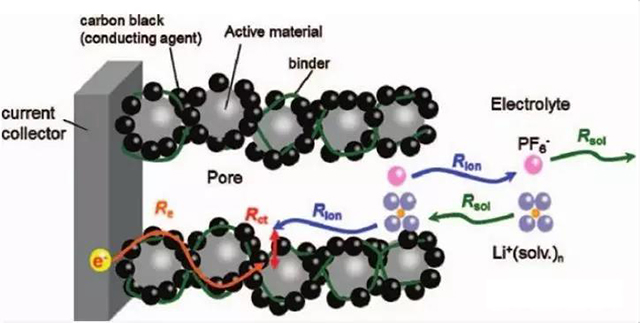
圖1-1 理想的電極微觀結構示意圖
那么,優化電極配方有什么理論指導或方法呢?以下介紹幾種具體的優化方法。
導電網絡逾滲理論模型
此理論是指只有當相鄰格子空隙被導電劑占據后,這些空隙才能形成一個導電網絡。假設格子空隙被導電劑占據的概率是P,占據概率P的增大可通過改變導電劑的形狀來實現。當P增大到某臨界值Pc時,就會發生逾滲轉變,體系電阻率會突然減小。導電劑的形態和種類眾多,顆粒狀炭黑和導電石墨是零維結構,而碳纖維和碳納米管是一維結構,石墨烯是二維片狀結構,導電劑的微觀結構特征與分布是影響導電性能的重要因素。
細小顆粒狀的零維結構的導電劑是點接觸、線狀一維結構導電劑是線接觸,片狀二維結構導電劑是面接觸。顆粒狀導電劑更容易在活性物質顆粒表面均勻分散,與活性物質緊密接觸,形成良好的短程電子通路,但是在整個電極的厚度方向不利于形成長程的電子傳輸通道。而一維結構的導電劑與活性物質難形成緊密接觸,短程電子傳導差,一維長鏈結構使長程電子傳導性能好。
石墨烯具有很高的電導率及二維超薄的結構特征,通過與活性物質的“面—點”接觸,使得很少含量的石墨烯就可以有效提高電極的電子電導率,但其分散困難,團聚的石墨烯會對電極內部鋰離子的傳輸產生阻礙,影響高倍率條件下電池性能的發揮。綜合利用各種形態導電劑的優點,采用多種結構的混合導電劑有利于形成完整的導電網絡
球狀導電劑的臨界值Pc(滲流閾值)比纖維狀導電劑大很多。因此,纖維狀的CNTs和VGCF作為導電劑時,由于其粒子長徑比較大,在格子逾滲理論模型中,1根CNIs或VGCF可同時占據多個相鄰空隙,而球狀的炭黑粒子1次只能占據1個空隙且只有相鄰空隙被占據后才能形成導電網絡。
因此,同等條件下,纖維狀的CNTs 和GCF導電劑形成網絡可能性比炭黑粒子的可能性大很多,如圖2所示。

圖1-2 片狀、顆粒狀和橢球纖維狀導電劑與活性物質結構示意圖
導電復合材料產生逾滲現象的原因是:隨著導電粒子濃度的增加,導電粒子之間開始相互接觸,當形成連續導電逾滲網絡時,材料的電導率突然迅速增加。根據這個理論可以用于指導優化電極配方中的導電劑含量。Kirkpatrick、Zallen等借用Flory凝膠理論描述導電網絡的形成,并提出經典統計的逾滲理論方程:

對于二維體系x的典型值為1.3;對于三維體系x為1.9,并推斷出,球狀粒子只有體積分數達到16%以上時,才會形成導電網絡。而電池中,炭黑類導電劑能夠相互聯通的滲流閾值一般認為是3%。實驗中,針對特定的材料體系,通過實驗可以確定滲流閾值。
Doyle/Fuller/Newman電池模型優化電極配方
基本模型描述如下,電極孔隙率計算公式為:
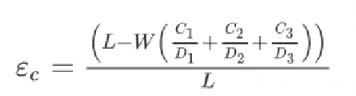
對于電極的電導率,根據以下公式計算:
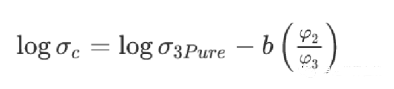
粘結劑和導電劑的體積分數比值,根據各自的真密度,可以轉化為重量比值:
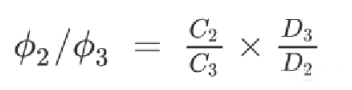
本文根據電化學模型,優化粘結劑和導電劑的比例。
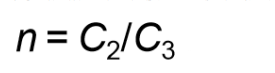
以上各式中,各母含義如下:
L是電極涂層厚度。
W是電極涂層單位面積的重量。
Dk是各組分的真密度,Ck是各組分的重量百分比,其中1代表活性物質,2代表粘合劑,3表示導電添加劑。
σc是電極電導率,σ3pure是純導電劑的電導率。
φ是電極涂層中各組分的體積分數,2代表粘合劑,3表示導電添加劑。
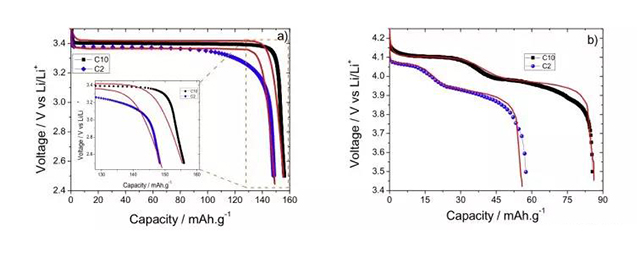
圖2-1模擬結果與實驗測試值比較一致,驗證了模型的有效性,可用于電池配方設計。
正極活性物質的電子電導率很低,電極中電子的傳導主要是由導電劑所組成的導電網絡承擔,因而導電網絡的完整性對電極的導電性能具有重要意義。 要在電極中形成完整的導電網絡,導電劑的添加量就必須達到一定量并且導電劑顆粒之間要形成有效接觸。首先,固定活性物質含量C1,改變粘結劑含量C2,和導電劑含量C3,即改變n值,研究電極配方的影響。
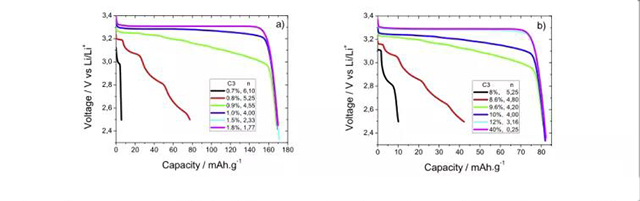
圖2-2a:LFP半電池,C1=95%,不同的導電劑含量C3(n不同)下,放電曲線
圖2-2b:LFP半電池,C1=50%,不同的導電劑含量C3(n不同)下,放電曲線
當C1=95%,C3低于1%(n <4)時,電池不穩定并且容量損失嚴重,而C3高于1%時,電池性能基本穩定,容量接近170mAh。當C1=50%時,閾值仍為n=4。結果表明,對于特定含量的活性材料C1,存在C3的最小值以維持低內阻并且沒有容量損失,即存在n的最大值。
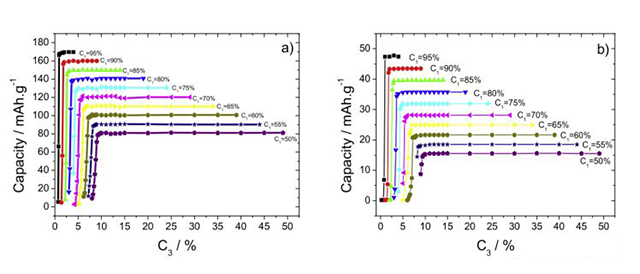
圖2-3 倍率1C時,不同活性物質含量C1下(a)Li/LFP和(b)Li/LMO半電池放電容量與導電劑含量C3的關系
然后,設定不同的活性物質比例C1,電極性能隨著導電劑含量C3的變化規律如圖2-3所示,系列模擬結果表明,存在一個最大值n=4,即粘結劑與導電劑的比例最大值為4,如表4所示。當n>4時電池保持良好的性能,當n<4時,電池性能急劇下降。
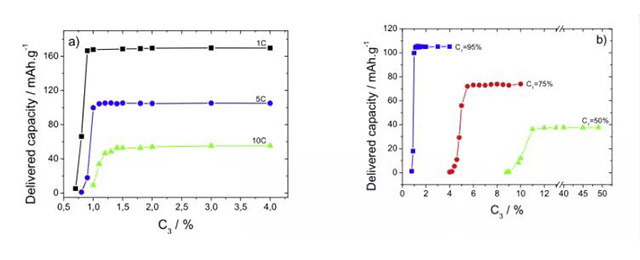
圖2-4 LFP半電池 a)C1=95%在1C、5C和10C下放電容量;b)C1=95%、75%和50%在5C下放電容量
當放電倍率增加時,要保持穩定的電池性能,導電劑含量相應要增加。即倍率增加,則C3增加,n降低,如圖2-4所示。
總結:對于任一活性材料,特定C1值時,最低阻抗轉折點對應最小值C3,比率n = 4。
對于C1 = 95%,在C3> 1%,對應于n <4時,離子電流密度的線性降低。在C3≤1%(n≥4)時,隨著離電極表面深度增加,鋰離子電流密度保持比較大,電荷交換比較少,電極反應少,這主要是電子傳輸沒有到達參與反應,插層反應更多地發生在靠近集流體一側。對于C1=50%,現象類似。
對于C1 = 95%,在C3> 1%,對應于n <4時,電子電流密度的線性增加。在C3≤1%(n≥4)時,隨著離電極表面深度增加,電子電流密度比較小,電子傳輸沒有到達參與反應,限制了插層反應。對于C1=50%,現象類似。
因此,本文得出結論:
•通過理論模擬優化鋰離子電池的正極配方。
•電極配方與活性材料類型無關。
•聚合物粘合劑/導電添加劑的比例應<4。
•正極的最佳成分應含有90%的活性物質。
•聚合物粘合劑和導電添加劑應在2%至8%之間。
另外,電極中粘結劑一般和導電劑混合在一起,使活性物質顆粒通過碳膠混合相連接在一起形成機械性穩定的整體,并確保電極與集流體之間具有足夠的粘結強度。粘結劑的含量主要影響電極的機械穩定性,但是同時會影響電極電導率,而且兩者往往相互矛盾。實際的電極配方還是非常復雜的,最后也沒有什么結論。
本文鏈接:http://www.qhgfjy.com.cn{dede:field.arcurl/}
諾信新聞,諾信公司新聞,鋰電池行業新聞,展會新聞









