鋰電池極片導電劑用量理論估算
一、導電劑作用
在鋰離子電池極片中,在活性物質的某一點發生脫鋰/嵌鋰反應時,極片內部涉及電子、鋰離子傳輸過程。例如放電時,在正極側活性物質顆粒表面某一點發生嵌鋰反應,進入固相顆粒內部:Li從負極通過電解液傳至正極,電子經外電路傳至正極集流體,然后通過電極中的導電劑網絡傳輸至電極表面,電子和鋰離子在正極顆粒/電解液界面發生電荷交換, Li得到電子,嵌入正極材料。如圖1所示,電化學反應發生必須滿足:鋰離子和電子都傳輸到達該點。因此,電子傳輸是極片中重要的步驟,電子傳導特性直接決定電化學性能。

圖1 正極極片內鋰和電子傳輸示意圖
極片設計中,活性物質,特別是正極材料電子電導率很低,導電劑網絡是電子傳輸的主要路徑。在進行鋰離子電池設計時我們應根據不同的活性物質材料、不同目的(改善倍率性能、循環性能、提高不可逆比容量)而選取與之相匹配的導電劑。導電劑的材料、形貌、粒徑、攪拌順序、添加量與不同類型導電劑的復合狀態都對鋰離子電池有著不同方面的影響。
二、導電劑理想分布狀態
導電劑在電極中的理想分布狀態如圖2中structure3所示:1)導電劑均勻分散,在活性物質顆粒表面形成導電薄層;2)導電劑與活性物質顆粒表面緊密接觸,使電子能夠有效參與脫/嵌鋰反應;3)導電劑之間相互連通導電,從集流體到每一個活性物質顆粒形成電子通路。
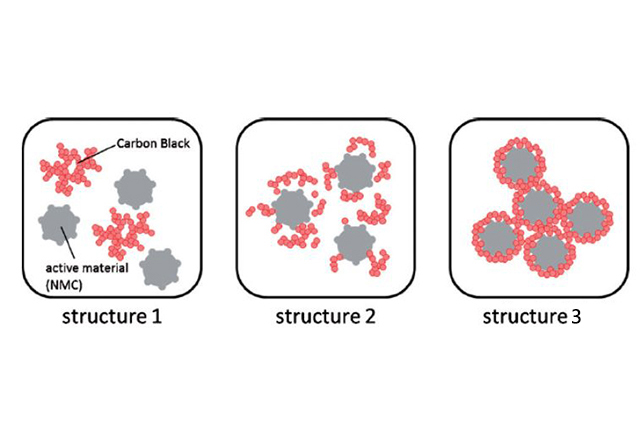
圖2 導電劑分布狀態
導電劑在電極中的作用是提供電子傳輸的通道,導電劑含量適當能獲得較高的放電容量和較好的循環性能,含量太低則電子導電通道少,不利于大電流充放電,會導致電極中活性物質利用率低;太高則降低了活性物質的相對含量,使電池比能量降低。
三、導電逾滲曲線
導電復合材料產生逾滲現象的原因是:隨著導電粒子濃度的增加,導電粒子之間開始相互接觸,當形成連續導電逾滲網絡時,材料的電導率突然迅速增加。根據這個理論可以用于指導優化電極配方中的導電劑含量,如圖3所示。但是,導電逾滲曲線一般也是通過實驗的方法確定的。
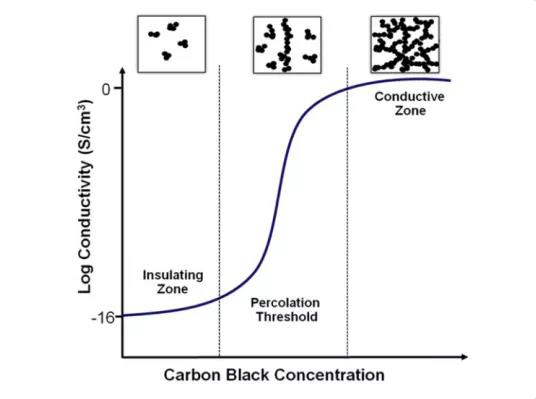
圖3 經典逾滲曲線
四、導電劑用量理論模型
根據前面對導電劑的理想分布狀態的描述,我設想了一個理論估算極片導電劑用量的方法,理解不對之處,請大家指正。
假設活性材料的比表面積為S(m2/g),理想狀態下,其表面上均勻包覆一層導電劑,如圖2所示,厚度為h(nm),那么每1g活性物質需要的導電劑體積為:
V=S*(h*10e-9)(m3)
再假設導電劑顆粒的直徑為d(nm),即顆粒狀SP導電劑的顆粒直徑,或者CNT的管徑等于d,而導電劑的密度為p(g/cm3)。
如果取h=d,那么每1g活性物質需要的導電劑質量為:
m2=(p*10e6)*V
=(p*10e6)*S*(d*10e-9)(g)
類似的,如果取h=2d,那么每1g活性物質需要的導電劑質量為:
m2=(p*10e6)*V
=(p*10e6)*S*(2*d*10e-9)(g)
即活性物質質量m1與導電劑質量m2比值為1/m2,這樣就確定了導電劑的用量。下面舉例,表1為高鎳正極材料的特性參數,NCA和NCM811比表面積分別為0.65m2/g,0.25m2/g。表2為導電劑特性參數,SP、CNT粒徑分別為40nm、5nm,如果導電劑密度為2.05g/㎝3。
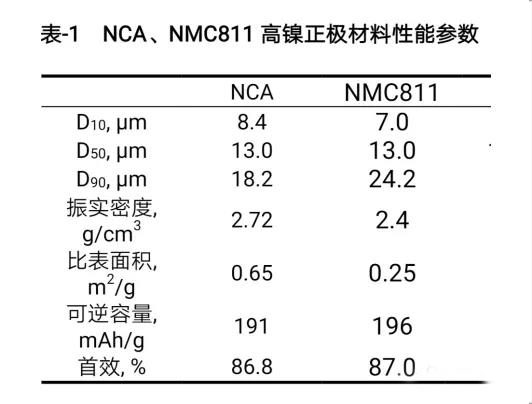
表1 NCA、NMC811高鎳正極材料性能參數

表2 常見導電劑參數
以導電劑sp為例,根據前面理論模型,如果h=d,則對于NCA正極,有:
m2=(p*10e6)*S*(d*10e-9)(g)
=(2.05*10e6)*0.65*(40*10e-9)(g)
=0.0533(g)
即NCA:SP=100:5.33。
對于NCM811正極,有:
m2=(p*10e6)*S*(d*10e-9)(g)
=(2.05*10e6)*0.25*(40*10e-9)(g)
=0.0205(g)
即NCM811:SP=100:2.05。
如果采用CNT,對于NCM811,則有
m2=(p*10e6)*S*(d*10e-9)(g)
=(2.05*10e6)*0.25*(10*10e-9)(g)
=0.0052(g)
即NCM811:CNT=100:0.52,而NCA:CNT=100:1.33
由此可見,導電劑的用量和活性材料的比表面積、導電劑材料的粒徑等有關。活性物質比表面積越大,導電劑粒徑越大,導電劑用量越多。CNT用量比SP少很多,但是CNT更難在活性物質顆粒表面形成包覆層。
文獻實驗結果表明,復合導電劑配方有利于電池性能的提升,其中顆粒狀導電劑主要是緊密包覆在活性物質顆粒表面,形成短程導電路徑,而一維導電劑鏈接各個顆粒,形成長程導電路徑。因此,顆粒狀導電劑還是可以根據以上理論模型估算用量。一維導電劑用量需要根據極片壓實密度確定。
五、理想導電網絡的實現方式
為了形成圖2所示的理想導電劑網絡分布,研究者開發了各種技術與工藝,包括電極漿料的制備方法,活性物質材料的設計等方面。
5.1、漿料球磨制備工藝
電極漿料球磨制備工藝能夠形成導電劑包覆在活性物質顆粒表面的結構。但是,球磨工藝容易造成材料結構的破壞,工業生產一般不使用,主要應用于實驗室漿料制備。
總之,與基于流體力學攪拌工藝相比,球磨工藝提供更小的活物質和導電劑團簇尺寸,同時也會破壞活物質和導電劑顆粒形貌。當活物質和導電劑顆粒本身形貌對電極性能有益時,球磨工藝并不好。
5.2、電極漿料干粉攪拌工藝
目前,先將漿料組分進行預先干粉混合(活物質/導電劑),然后將這些混合粉體分散到粘合劑溶液中,這成為一種攪拌工藝趨勢,如圖4所示。
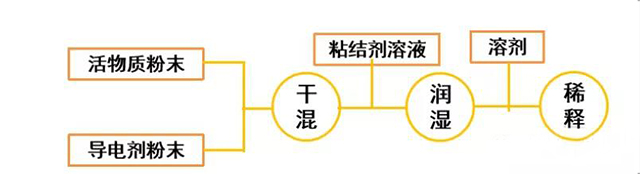
圖4 干粉攪拌工藝
在活性物質 / 導電劑的高強度混合過程中,活性物質顆粒被薄碳層覆蓋。干混后電極性能的改善與電子通路的增加有關,較小的導電劑顆粒在較大活性物質顆粒表面均勻分布。這種電子通路的改善與混合強度有關,低能量干粉混合的效果不顯著。
因此,近年出現高強度干粉混合工藝改善漿料和電池特性的報道。圖5為高強度剪切混合設備Nobilta™結構示意圖,攪拌拐和壁的間隙3mm,內外壁之間有一層水套冷卻高速分散中產生熱量導致的溫升。
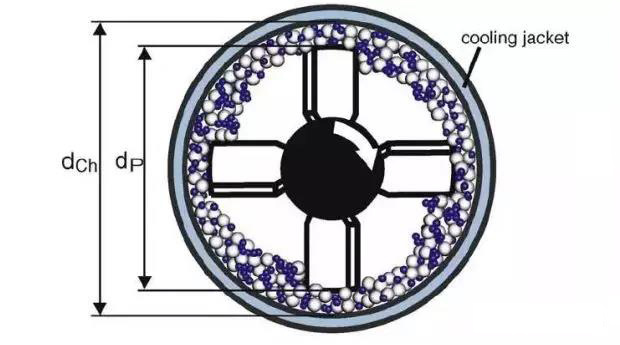
圖5 高強度剪切混合設備Nobilta示意圖
高強度的干粉剪切分散具有兩個方面的作用:一方面,高的剪切力能夠使導電劑團聚體充分破碎分散,另一方面,高速分散作用下,干粉攪拌能夠實現微觀上的混合,在較大的活物質顆粒表面沉積形成一層由細小的分散開的導電劑沉積層,從而形成良好的導電網絡。
但是,如果強度太高,或者時間太長,導電劑粉碎成細小顆粒,雖然增加了導電劑與活物質之間的接觸和分散效果,但是破壞了導電劑網絡的長距離導電性能,所制備的極片電阻會增加,相應的電池性能反而會變差
5.3、導電劑高速剪切分散技術
對于比表面積特別大,容易團聚的導電劑,研究人員開發了很多高速分散技術,努力實現這些導電劑的實際應用。以下主要介紹幾種高速分散技術與設備。
(1)真空浸潤分散技術
設備內形成真空環境,粉體打散-浸潤-混合-分散在幾秒鐘內完成:
①加料系統和均勻給料器,控制粉料投入速度;
②經過粉體分散裝置,粉體在真空環境下被分散成霧狀,粉體內部氣體大部分被吸出;
③在固液混合區,粉體均勻浸入高速液流中,并迅速的溶解;
④在分散區出口壓力環境下,溶液壓入微粒空穴中,形成穩定的懸浮液。
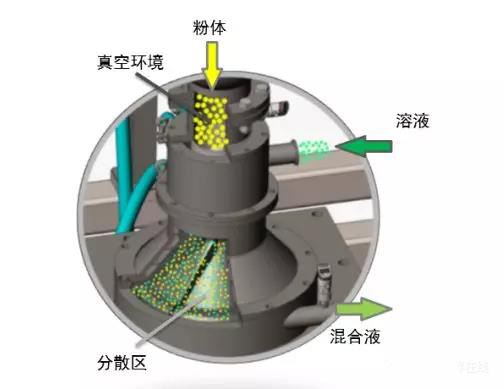
圖6 真空浸潤分散技術
(2)Eirich Mixer攪拌機
料桶旋轉帶動漿料轉動,葉片高速旋轉對漿料剪切分散。基本流程:把所有的粉末狀原料先進行1到2分鐘干混在混合均勻后陸續加入1/4粘結劑使原料粒化,再加入1/4進行捏合,最后添加剩余的粘結劑進行分散。整個過程僅用時15分鐘左右。

圖7 Eirich Mixer攪拌機
(3)FILMIX攪拌機
攪拌原理為圓筒狀的PC轉子高速旋轉,從容器底部送來的漿料沿著容器旋轉,持續輸送漿料后,漿料被離心力強行擠壓到容器壁上,形成薄膜高速旋轉,產生巨大的剪切力是顆粒分散細化,并在容器壁面上下方向和與PC轉子旋轉的2個運動形成復雜流場,短時間內均一分散,連續設備溫升比較嚴重。

圖8 FILMIX攪拌機
(4)管式靜態混合器
由一系列安裝在空心管道中的不同規格的混合單元進行的。由于混合單元的作用,使流體時而左旋向,時而右旋向,不僅將中心液流推向周邊,而且將周邊流體推向中心,從而造成良好的徑向混合效果。與此同時,流體自身的旋轉作用使流體相互混合,這種完善的徑向環流混合作用,使物料混合均勻

圖9 管式靜態混合器
5.4、材料導電包覆
另外,還有人從活性材料設計的角度考慮,開發導電碳層包覆的材料,有利于提高材料的電導率,同時還可以形成材料保護層,避免與電解液反應。
總之,鋰離子電池的導電劑是非常重要的,導電劑材料本身的設計與制備,導電劑的利用技術,如配方、分散工藝等都需要開展研究工作,充分發揮其作用,提升電池性能。
本文鏈接:http://www.qhgfjy.com.cn{dede:field.arcurl/}
諾信新聞,諾信公司新聞,鋰電池行業新聞,展會新聞
下一篇:溫度對鋰離子電池極片工藝的影響









